Capítulo 57 n-de-1
57.1 Ensaio n-de-1
57.1.1 O que são ensaios n-de-1?
Ensaios n-de-1 são delineamentos experimentais em que um único paciente recebe, em períodos alternados, duas ou mais intervenções (ex.: tratamento A e tratamento B).471
Cada ciclo é formado por dois períodos (AB ou BA), cuja ordem é randomizada, garantindo controle temporal e redução de vieses.471
O foco está na comparação intraindivíduo, permitindo avaliar diretamente se o paciente em questão responde melhor a uma intervenção.471
57.1.2 Quando é apropriado conduzir ensaios n-de-1?
Doenças crônicas estáveis, em que o desfecho pode ser observado repetidamente.471
Condições raras ou com grande heterogeneidade de resposta entre pacientes.471
Situações clínicas de incerteza, quando se deseja personalizar o tratamento.471
Ensaios n-de-1 devem ser utilizados principalmente para apoiar decisões clínicas sobre o cuidado de um paciente individual, e não para estimar efeitos médios em populações.472
Eles são uma opção viável quando se lidam com intervenções de muito baixo volume, como em doenças raras ou ultrarraras, nas quais ensaios tradicionais são inviáveis.472
Uma ampla variedade de tecnologias em saúde pode ser avaliada por ensaios n-de-1, incluindo medicamentos, dispositivos, intervenções dietéticas e comportamentais, desde que atendam aos critérios de início de efeito e ausência de efeitos residuais prolongados.472
Para que uma tecnologia seja adequada a um ensaio n-de-1, seu efeito deve surgir em um intervalo de tempo que possa ser medido dentro de um período de estudo factível.472
Tecnologias avaliadas em ensaios n-de-1 não devem apresentar efeitos de “carryover” prolongados; quando isso não é possível, é necessário empregar estratégias adequadas de washout.472
Ensaios n-de-1 são particularmente úteis para avaliar tecnologias caras ou com efeitos adversos relevantes, permitindo verificar se, para aquele paciente específico, os benefícios superam os riscos e os custos.472
Esses ensaios podem responder perguntas sobre se o tratamento funciona, se funciona melhor do que alternativas existentes, qual tratamento é mais adequado para um paciente específico ou se a resposta ao tratamento varia entre indivíduos.472
57.1.3 Qual a relevância dos ensaios n-de-1?
Os ensaios n-de-1 permitem decisões clínicas personalizadas e baseadas em evidência direta.471
Quando combinados, podem gerar estimativas comparáveis às de ensaios clínicos convencionais, mantendo o foco centrado no paciente.471
Representam uma alternativa metodológica robusta para cenários de incerteza terapêutica.471
57.2 Aspectos metodológicos
57.2.1 Quais são os principais aspectos do delineamento de ensaios n-de-1?
A escolha do desfecho primário deve ser guiada diretamente pela pergunta clínica que o ensaio pretende responder.472
Sempre que possível, recomenda-se combinar desfechos relatados pelo paciente com medidas mais objetivas, especialmente em ensaios envolvendo tratamentos caros ou de maior risco.472
Ensaios n-de-1 podem avaliar não apenas eficácia, mas também outros desfechos relevantes para o paciente, como efeitos adversos, qualidade de vida e preferências pessoais.472
O comparador do tratamento deve ser escolhido de acordo com a pergunta de pesquisa, podendo ser placebo, tratamento ativo ou cuidado padrão.472
O foco do tratamento em um ensaio n-de-1 pode ser a doença em si, sintomas específicos, efeitos colaterais ou a satisfação do paciente com a intervenção.472
Na prática, a maioria dos ensaios n-de-1 compara duas tecnologias; a comparação de três ou mais aumenta significativamente a complexidade operacional.472
O número de períodos do estudo deve equilibrar precisão e viabilidade, considerando duração total do ensaio e carga para o paciente.472
O cegamento deve ser utilizado sempre que viável; quando não for possível, outras formas de minimizar viés, como avaliação cega de desfechos, são recomendadas.472
A randomização da sequência de tratamentos é recomendada, preferencialmente em blocos, para reduzir vieses e efeitos relacionados ao tempo.472
Análises interinas podem ser consideradas, permitindo interromper o ensaio precocemente caso haja evidência suficiente de benefício ou dano.472
Quando há risco de efeitos residuais entre períodos, devem ser empregados washout tradicionais ou washout ativo, sempre ponderando rigor metodológico e segurança do paciente.472
A interpretação dos resultados não deve se basear apenas em significância estatística; a relevância clínica do efeito é essencial.472
A análise central de um ensaio n-de-1 é a análise intra-paciente, que avalia se houve um efeito clinicamente importante para aquele indivíduo.472
Quando vários ensaios n-de-1 são conduzidos, seus resultados podem ser combinados para estimar efeitos médios e avaliar a consistência entre pacientes.472
O envolvimento de pacientes e do público é fundamental em todas as etapas do ensaio n-de-1, incluindo planejamento, definição de desfechos, interpretação, disseminação e implementação dos resultados.472
57.2.2 Quantos períodos são usualmente utilizados?
A mediana observada em ensaios recentes foi de 6 períodos (intervalo interquartil 4–8).473
Esse número parece representar um equilíbrio entre maior precisão estatística (mais períodos) e viabilidade prática e adesão do paciente (menos períodos).473
57.2.3 Como é feita a randomização?
A ordem dos tratamentos em cada ciclo é definida aleatoriamente (ex.: AB, BA, AB…).471
A randomização reduz viés de período e efeito de expectativa.471
57.2.4 Quais perguntas de inferência podem ser respondidas?
Q1: Há efeito do tratamento dentro dos ciclos de um paciente?471
Q2: Qual é o efeito médio observado nos pacientes estudados?471
Q3: O efeito é homogêneo ou heterogêneo entre pacientes?471
Q4: Qual é o efeito específico em cada paciente individual?471
Q5: Qual é o efeito esperado em populações semelhantes?471
57.3 Análise de dados
57.3.1 Como são feitas as análises?
Comparações intraindivíduo (testes pareados ou estimativas de efeito médio por paciente).471
Combinação de múltiplos n-de-1 por meio de meta-análises ou modelos mistos para inferências em nível populacional.471
57.3.2 Quais métodos estatísticos têm sido utilizados recentemente?
- Diversos métodos têm sido aplicados, incluindo testes t, modelos de regressão, modelos Bayesianos, testes não paramétricos, modelos mistos, e inspeção gráfica.473
57.3.3 É adequado utilizar P-valores em ensaios n-de-1?
Em ensaios n-de-1 a interpretação deve ser cautelosa, pois um P-valor não significativo não exclui a presença de efeito clinicamente relevante.473
Estimativas pontuais e intervalos de confiança podem ser mais informativos para decisões clínicas individuais.473
57.3.4 Como os dados de ensaios n-de-1 podem ser visualizados?
- Trellis plot, no qual cada painel representa um paciente e cada ponto corresponde a um ciclo, plotando-se o desfecho sob B no eixo Y e sob A no eixo X. A linha de identidade indica igualdade entre os tratamentos; a concentração de pontos acima e à esquerda dessa linha sugere maior efeito do tratamento B.471
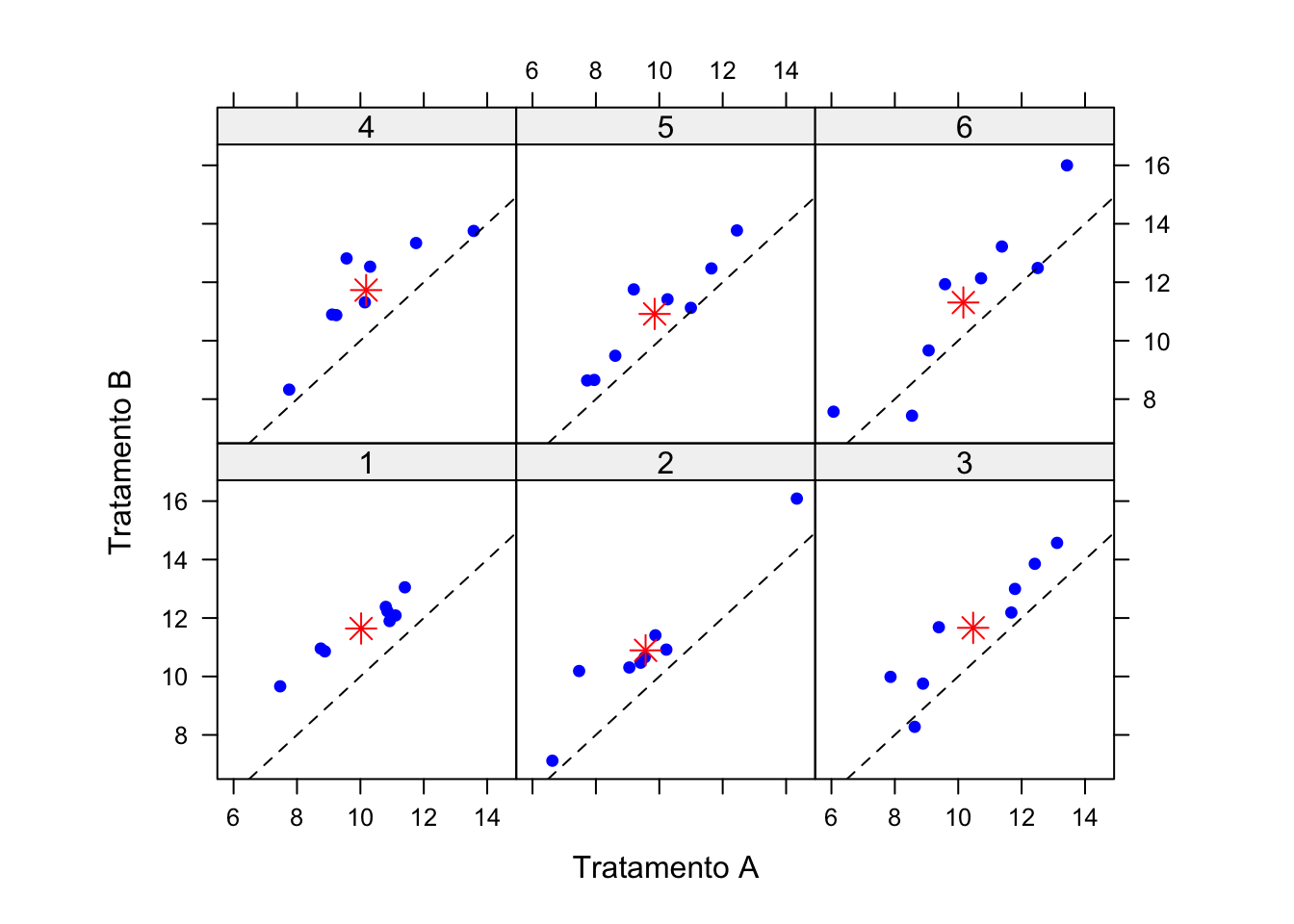
Figura 57.1: Trellis plot para dados simulados de ensaio n-de-1. Cada painel representa um paciente, cada ponto azul um ciclo, e o asterisco vermelho indica a média dos ciclos para aquele paciente. A linha tracejada representa a linha de identidade (igualdade entre tratamentos).
57.3.5 Quais métodos estatísticos são usados na análise?
A hipótese nula assume ausência de diferença entre os tratamentos para todos os pacientes, implicando independência das diferenças entre A e B e permitindo a agregação dos dados entre ciclos e indivíduos.471
Os dados são reduzidos a diferenças emparelhadas por ciclo e paciente, resultando em uma única amostra de diferenças.471
As diferenças observadas podem ser analisadas por meio de um teste t de uma amostra ou Mann-Whitney-Wilcoxon.471
57.4 Abordagem meta-analítica
57.4.1 Como um conjunto de ensaios n-de-1 pode ser analisado conjuntamente?
Ele pode ser tratado de forma análoga a uma meta-análise de ensaios clínicos independentes, utilizando métodos e softwares padrão com pequenas adaptações.471
Devido ao pequeno número de graus de liberdade por paciente, a estimativa ingênua de variâncias é inadequada, sendo necessário assumir variância intraindivíduo constante entre pacientes e utilizar uma variância agrupada.471
A variância agrupada é estimada a partir da soma dos quadrados corrigida das estimativas individuais, dividida pelo total de graus de liberdade, produzindo uma estimativa comum da variância intraindivíduo.471
57.4.2 Por que a meta-análise com efeitos aleatórios produz intervalos de confiança mais amplos?
- Porque ela estima um efeito de tratamento aplicável a uma população mais ampla e “semelhante”, tratando os pacientes estudados como uma amostra aleatória e incorporando a variabilidade entre indivíduos à incerteza do efeito estimado.471
57.4.3 Qual é a principal vantagem da abordagem meta-analítica?
- A vantagem é responder a uma pergunta inferencial mais relevante, sobre efeitos esperados em populações futuras.471
57.5 Limitações e cuidados
57.5.1 Quais são os principais desafios dos ensaios n-de-1?
Baixo poder estatístico quando poucos ciclos são realizados.471
Necessidade de períodos de washout para evitar efeito de carry-over.471
Interpretação dependente de pressupostos sobre homogeneidade ou heterogeneidade dos efeitos.471
Em amostras muito pequenas, pode ser necessário usar variâncias externas ou modelos mistos.471
A abordagem meta-analítica assume forte similaridade entre os pacientes estudados e a população-alvo.471
Ferreira, Arthur de Sá. Ciência com R: Perguntas e respostas para pesquisadores e analistas de dados. Rio de Janeiro: 1a edição,